重庆代孕价格
关于β受体阻滞剂,《JAMA》有话说!
心衰是各种心血管事件的最终结果和各种心脏异常的累积效应,最终导致心脏泵功能下降。
心衰越重,死亡风险越高。现代研究认为交感神经系统和肾素血管紧张素系统的激活是心衰的主要发病机制。
β受体阻滞剂(β-B)通过有效拮抗交感神经系统、肾素-血管紧张素-醛固酮系统(RAAS)和过度激活的神经体液因子,在心血管疾病的恶性循环链中起到重要的阻断作用,从而延缓或逆转心肌重构,发挥改善内源性心肌功能的“生物学效应”。
β-B在治疗3个月后可改善患者心功能,提高左心射血分数(LVEF),治疗6个月后还能降低心室肌重量和容量,延缓或逆转心肌重构。
病情相对稳定的射血分数降低的心衰(HFrEF)患者均应使用β-B,除非有禁忌证或不能耐受。因为缺乏足够的循证医学证据,HFpEF的临床研究均未能证实β-B可改善射血分数保留的心衰(HFpEF)患者的预后。
在衰竭心脏中,β1受体信号传递是心脏病理变化的主要通路,治疗心衰最重要的是阻滞β1受体。高选择性β1受体阻滞剂可逆转心室重构或降低死亡的危险性。
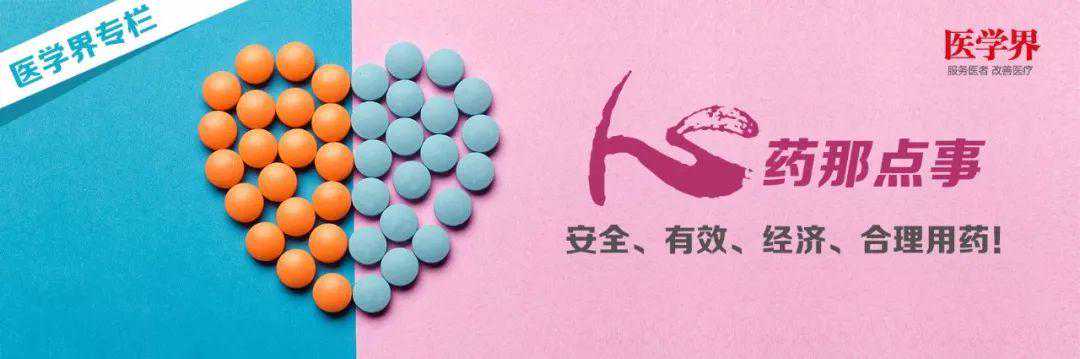
同时,高选择性β1受体阻滞剂因其不阻断β受体,产生的不良反应(ADR)较小,更易于让患者接受。因此,现常用的β-B包括琥珀酸美托洛尔、比索洛尔及卡维地洛等,其药代动力学特点及作用位点见下表1:
表1常用β受体阻滞剂代动力学特点及作用位点
4项经典的针对HFrEF患者的大型临床试验(MERIT-HF、CIBISⅡ、USCarvedilolHFStudy、COPERNICUS)已证实,与安慰剂相比,β-B降低全因死亡风险34%~65%、降低猝死风险41%~44%、降低心血管死亡或住院风险27%~38%,并提高患者的心功能分级和生活质量。
但《JAMAnetworkopen》最新研究却显示,使用β-B的心衰患者,住院风险增加74%。在所有受试者当中,22.7%发生心衰住院,13.0%发生心血管疾病(CVD)死亡。HFpEF患者住院风险更高,但在射血分数在45%至49%之间的患者风险不会增加。

那么,如何使用β-B治疗HFrEF才规范?
01把握β-B
在心衰患者中的合理使用
HFrEF确诊后应在病情相对稳定时尽早使用,推荐应用上述三种β-B。纽约心脏协会(NYHA)心功能Ⅳ级患者应在血流动力学稳定后,遵循专科医生监护指导使用。
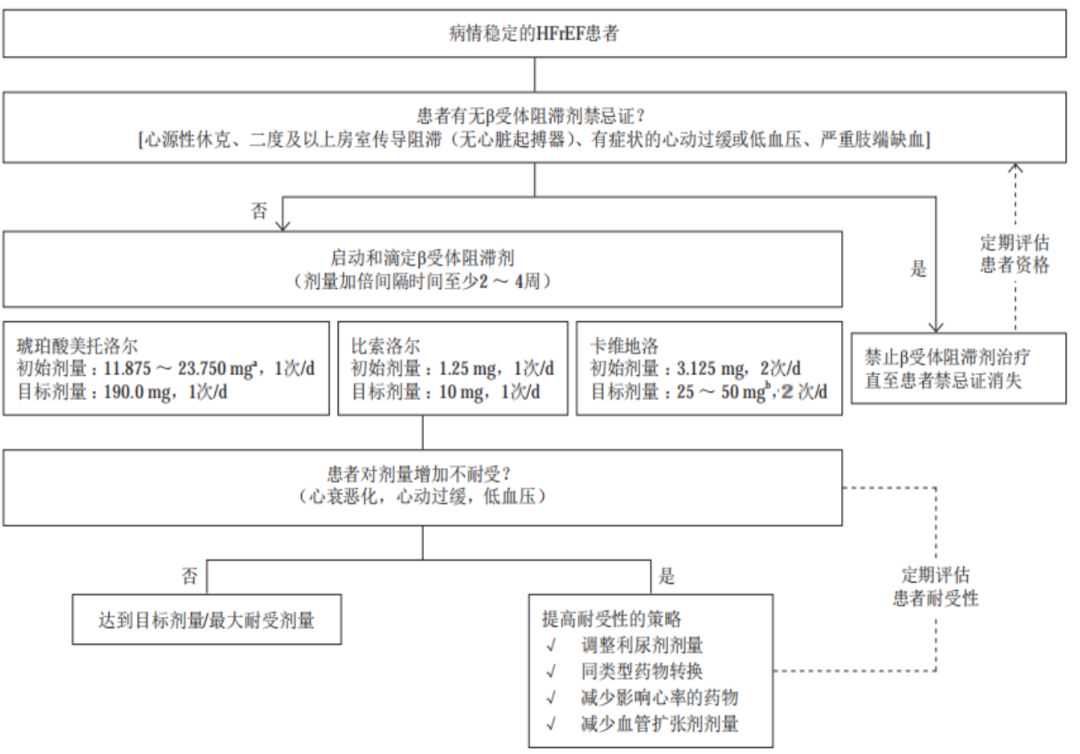
图1HErEF患者β-B应用方法
注:目标剂量是在既往临床试验中采用、达到证实有效的剂量。
因β-B的负性肌力作用可能诱发和加重心衰,治疗心衰的生物学效应需持续用药2~3个月才逐渐产生,故起始剂量要小,每隔2~4周可使剂量加倍,逐渐达到指南推荐的目标剂量或最大可耐受剂量,并长期使用。
02如何确定目标剂量?
静息心率是评估心脏β受体有效阻滞的指标之一,通常静息心率降至60次/min的剂量为β受体阻滞剂应用的目标剂量或最大可耐受剂量。
中国人群个体差异很大,因此β-B滴定的剂量及过程需个体化,要密切监测心率、血压、体重、呼吸困难、淤血症状及体征。常用β受体阻滞剂初始剂量及目标剂量推荐,见表2:
表2常用β-B初始剂量及目标剂量推荐表

注:a:NYHA心功能Ⅱ-Ⅲ患者推荐剂量为23.75mg;NYHA心功能Ⅳ级推荐剂量为11.875mg;b:体重≤85kg,推荐目标剂量为25mgbid;体重85kg,推荐目标剂量为50mgbid。
β-B可能致液体潴留,因此有液体潴留或最近曾有液体潴留患者,必须同时使用利尿剂。
《中国心衰指南2014》指出,血管紧张素转换酶抑制剂+β-B为治疗心衰的“黄金搭档”,如果再加醛固酮拮抗剂(螺内酯),则为“金三角”治疗方案,可明显降低心衰死亡风险。
在慢性心衰急性失代偿时,可继续维持使用,心动过缓(50~60次/min)和血压偏低(收缩压85~90mmHg)患者可减少剂量,严重心动过缓(<50次/min)、严重低血压(收缩压<85mmHg)及休克患者应停用,但在出院前应再次启动β-B治疗。
03β-B所致
ADR的类型及注意事项
ADR常在药物应用初期或加量过程中出现。
心动过缓和房室传导阻滞
因β-B对心脏的负性频率和负性传导所致。临床应根据患者心率下降程度决定药物剂量,应注意药物相互作用的可能性,停用其他可致心动过缓药物。
低血压
一般出现于首次剂量或加量的24~48h内。若无症状,无需处理,重复用药后常可自动消失。与ACEI在不同时间服用可降低低血压发生风险。
处理方法:首先停用硝酸酯类药物、CCB或其他不必要的血管扩张剂。容量不足者利尿剂应减量。低血压伴低灌注者β-B减量或停用,并重新评估患者临床情况。
液体潴留和心衰恶化
每日称体重,如在3d内体重增加>2kg,应立即增加利尿剂剂量。
若心衰症状轻或中度加重,应增加利尿剂剂量。如病情恶化与β-B应用或加量相关,宜减量或退回至前一剂量。
应积极控制加重心衰的诱因,并加强各种治疗措施,必要时可短期静脉应用正性肌力药,磷酸二酯酶抑制剂较β受体激动剂更合适,因后者的作用可被β-B拮抗。
无力
多数数周内缓解,某些较严重需减量。如无力伴外周低灌注,则需停用β-B,稍后再重新应用或改用其他β-B。但心衰患者出现无力是多因素的,应注意考虑其他原因造成的疲劳。
增加气道阻力
当患者使用非选择性β-B时,由于β受体被阻断,支气管收缩,增加呼吸道阻力,诱发或加重支气管哮喘的急性发作,因此禁用于支气管哮喘和慢性阻塞性肺疾病肺疾病患者。
但对于慢性左心室功能不全、急性心梗伴发肺部疾病或肺部症状较轻患者可选择应用β1受体选择性较高的药物,用药后密切观察患者呼吸道症状,如无明显不适,可逐渐增加剂量,并长期治疗。
必须提出的是,这种对β1受体的高选择性也是相对的,当使用剂量较大时,仍可表现出对β受体的阻断作用。
加重外周循环性疾病
对本身存在闭塞性外周血管病患者使用β-B会加剧外周血管收缩,导致肢体温度降低、肢端苍白、疼痛及间歇性跛行等症状加重。原因在于使用β-B后,患者心输出量降低,外周血管收缩,肢体循环障碍加重。
低血糖反应
理论上讲,与糖脂代谢密切相关的为β受体,故β-B对β1受体的选择性越高,其对糖代谢的影响越小,但随着用药剂量的增大,选择性β1受体阻滞剂仍然存在剂量依赖性的β2受体阻断作用。
另外,需警惕β-B可引起外周血管痉挛导致外周肢体发冷,掩盖低血糖反应。
脂质代谢异常
大剂量β-B长期治疗,可明显抑制β受体,继而抑制了脂蛋白脂肪酶和卵磷脂胆固醇脂酰基转移酶的活性,产生对脂质代谢的不良影响,临床上表现为血甘油三酯、胆固醇升高、高密度脂蛋白胆固醇降低。
对β受体的阻断是引起脂质谱异常的主要原因,故患者可选择β1高选择性的受体阻滞剂来减轻脂质代谢异常。
撤药综合征
长期使用β-B可使受体上调,如突然撤药,可加重原病情。
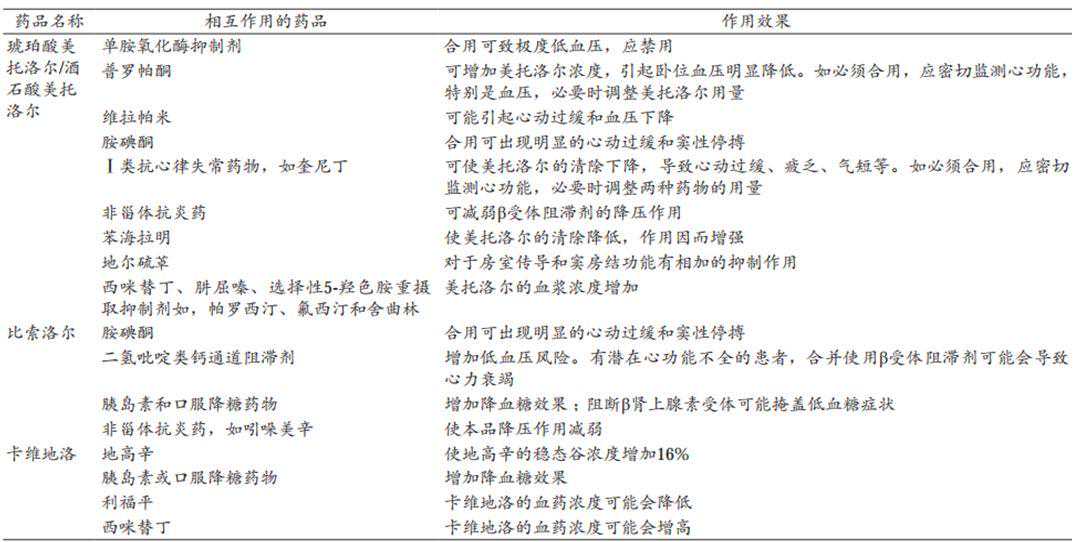
表3β受体阻滞剂与其他药物间相互作用
04ADR的防治
长期用药时应定期监测心率、血压、血糖、心电图、X线检查、心功能、肝功能、肾功能和血常规等。
β-B的心血管保护作用主要因阻断β1受体,对支气管、外周血管、糖脂代谢及性功能的不良影响主要是由于β受体被阻断。因此,在多数临床情况下,应尽量选用高选择性β1受体阻滞剂。
β1受体阻滞剂的心脏选择性与剂量有关,剂量大时选择性会减弱甚至消失,因此应根据临床情况使用适当剂量药物。
因患者对药物耐受性存在个体差异。β-B一般从小剂量开始,根据患者耐受情况逐步上调剂量。
ADR常发生在治疗早期,一般不妨碍长期用药。在出现ADR时,应及时适当处理,通常很少遗留长期或不可逆性严重损害。但若在长期服用时突然停药,易致病情恶化或增加猝死风险,故应逐渐减量后停药。
改善生活习惯:如久坐或久躺后缓慢起身、避免抽烟饮酒等。
参考文献:
[1]心力衰竭合理用药指南(第2版).国家卫生计生委合理用药专家委员会,中国药师协会.
[2]β受体阻滞剂在心血管疾病中应用的专家共识
[3]中国心力衰竭诊断和治疗指南
[4]黎镇赐,β受体阻滞剂常见不良反应及处理对策.中华高血压杂志,2012,20(5):419-420.
[5]施仲伟.β受体阻滞剂的不良反应及预防处理对策.医学研究杂志,2013,42(4):4-5.
[6]郭雨龙,刘爽.β受体阻滞剂对心血管病患者糖代谢的影响.心肺血管病杂志,2015,34(5):405-410.
[7]魏盟,李菁.正确评价β受体阻滞剂的选择性及其临床研究.中华高血压杂志2013,21(7):622-625.
本文首发:医学界心血管频道
审稿老师:武德崴北京航天总医院
版权申明
本文原创如需转载请联系授权
--



